
Impfstoffe [20a]
Mit Verfügbarkeit eines Impfstoffs kann die Pandemie wirksam gebremst werden. Gegen das Corona-Virus SARS-CoV-2 sind nach kurzer Zeit weit über 200 Impfstoffprojekte angelaufen. Forschungsinstitute und Unternehmen arbeiten mit Hochdruck an der Entwicklung eines Mittels gegen den Erreger von COVID-19. Aktuell sind in den USA und der EU zwei RNA-Impfstoffe zugelassen: Das Vakzin BNT162b2 von BioNTech/Pfizer [21d] und das Vakzin mRNA-1273 von Moderna [21j]. Darüber hinaus hat in Großbritannien der Vektorimpfstoff ChAdOx1 nCoV-19 der Firma AstraZeneca eine Notfallzulassung erhalten [21d]; die Zulassung in der EU erfolgte am 29.01.2021 [44]. Der vom Gamaleja-Institut für Epidemiologie und Mikrobiologie in Moskau entwickelte Vektorimpfstoff Gam-COVID-Vac (bekannt unter dem Namen Sputnik V) wird bereits seit Anfang Dezember 2020 in der russischen Bevölkerung verimpft und hat mittlerweile in mehreren Ländern eine Notzulassung erhalten [21m]. Eine Beantragung der Zulassung in der EU ist nach Angabe des russischen Direktinvestmentfonds geplant [21n]. Ende Februar 2021 erhielt mit Ad26.COV2.S von Janssen (einem Tochterunternehmen von Johnson & Johnson) ein weiterer Vektorimpfstoff eine Zulassung in den USA [21p]. Es ist das erste Vakzin, das in klinischen Studien nur eine Dosis benötigte, um die Immunisierung herzustellen [21p,q]. Die Zulassung in der EU wurde von Johnson & Johnson bereits bei der EMA beantragt [21q] und am 11.03.2021 erteilt [48].
Offizieller Impfstart in Deutschland war am 27.12.2020 mit dem Impfstoff der Firmen BioNTech/Pfizer [21e] .
Bei den zugelassenen RNA-Impfstoffen und Vektorimpfstoffen handelt es sich um Totimpfstoffe, d.h. sie enthalten keine vermehrungsfähige Erreger- oder Erregerkomponenten.
Bei der Impfstoffentwicklung werden aktuell 3 strategische Ansätze verfolgt:
- Inaktive Viren:
Der Erreger wird außerhalb menschlicher Zellen vermehrt und anschließend inaktiviert. Aus dem inaktivierten Virus wird im Anschluss der Impfstoff produziert. Hierbei werden Wirkverstärker hinzugefügt (z.B. Aluminiumhydroxid), um die Immunzellen zusätzlich zu stimulieren. Durch Präsentieren des gesamten Virus lösen Ganzvirusimpfstoffe eine breitere Immunantwort aus. Neben der Produktion von Antikörpern gegen das Spike-Protein werden auch andere Komponenten des Immunsystems angeregt, u.a. die als weiße Blutzellen bekannten T-Lymphozyten. Der im Zulassungsprozess befindliche Impfstoffkandidat VLA2001 der Firma Valneva enthält inaktive Sars-Cov-2-Viren, die in aus Nierenzellen der grünen Meerkatze abgeleiteten Zelllinien gezüchtet wurden [21r]. - Virus-Fragmente (Untereinheit-Impfstoffe): Das Immunsystem des Patienten „lernt“ das Virus zu erkennen abzuwehren, indem man dem Körper anders statt kompletter, inaktivierter Viren lediglich Virus-Fragmente zuführt. Der auf diesem Wirkprinzip beruhende Impfstoff NVX-CoV2373 der Firma Novavax [21s] ist am 20.12.2021 von der EMA zur Zulassung empfohlen worden. Das Präparat wurde bereits im November 2021 unter dem Namen Covovax in Indonesien zugelassen.
- Vektorimpfstoffe: Fragmente des Erbmaterials von SARS-CoV-2 wird in andere, abgeschwächte Viren (z.B. Masern- oder Influenzaviren), die für den Patienten ungefährlich sind, gebracht. Über diese sogenannten Vektorviren nehmen die Körperzellen die Erbinformationen in die Zelle auf, und der Körper entwickelt eine Immunität gegen das Virus. Der am 30.12.2020 in Großbritannien zugelassene Impfstoff, der von Astra-Zeneca zusammen mit der Universität Oxford entwickelt wurde, basiert auf diesem Prinzip. Es enthält das nicht replikationsfähige Erkältungsvirus (ChAdOx1), welches bei Schimpansen auftritt. Gegenüber den Vazinen der Firmen BioNTech/Pfizer und Moderna zeigte es in den bisherigen Studien mit 70% zwar geringere Wirksamkeit, ist aber deutlich günstiger herstellbar und einfacher zu verabreichen [21h]. Astra-Zeneca plant eine Untersuchung, inwieweit die Wirksamkeit durch Kombination mit weiteren Vektorimpfstoffen wie den russischen Sputnik-V-Vakzinen erhöht werden kann [21i].
Der Vektorimpfstoff Ad26.COV2.S von Janssen (Johnson & Johnson) basiert auf dem gleichen Erkältungsvirus wie der AstraZeneca-Impfstoff [21p]. Die klinischen Studien von Johnson & Johnson fokussierten von Beginn an auf die Immunisierung nach der 1. Dosis. Hierbei wurde eine Wirksamkeit von 67% nachgewiesen [21p].
Der in Russland entwickelte Vektorimpfstoff Sputnik V zeigt gem. der 2021 in „The Lancet“ veröffentlichten Ergebnisse eine Schutzwirkung von rund 92% [21o]. Die höhere Wirksamkeit gegenüber dem Vakzin von Astra-Zeneca wird dadurch erklärt, dass beim russischen Impfstoff Impfdosis 1 und 2 unterschiedliche Erkältungsviren enthalten. Hierdurch wird eine Verminderung der Auffrischungswirkung durch Antikörper, die gegen das Erkältungsvirus der 1. Dosis gebildet werden, verhindert [21n].
Bemerkenswert ist auch eine Studie des Forscherteams von A.O. Hassan, in denen Mäusen ein Vektorimpfstoff gegen SARS-CoV-2 verabreicht wurde. Dieser führte sowohl bei intramuskulärer als auch bei nasaler Anwendung zu einem Schutz der Tiere, wobei letztere eine höhere Schutzwirkung zeigte [21g]. Trotz der bereits zugelassenen m-RNA-Vakzine (s. Nukleinsäuren) sind Nasalimpfstoffe aufgrund der erleichterten Impfdurchführung und offener Fragen hinsichtlich der Infektiosität geimpfter Personen weiterhin von hohem wissenschaftlichen Interesse. - Nukleinsäuren: Dem Patienten werden Biomoleküle (die sogenannten Nukleinsäuren wie z.B. RNA), die Träger der Erbinformation des Virus sind, verabreicht. Nach Aufnahme in die Körperzellen werden die Nukleinsäuren in Proteine übersetzt. Von diesen lernt das Immunsystem, wie die Oberfläche des Virus aussieht und kann ihn abwehren. Dieser Ansatz liegt den m-RNA-Impfstoffen der Firmen BioNTech/Pfizer [21e] und Moderna [21f] zugrunde. Beide Impfstoffe werden intramuskulär verabreicht.
Die Wirkungsweise, Vor- und Nachteile der heute bekannten Impfstoffarten sind in dem nachfolgenden Schema zusammengefasst.
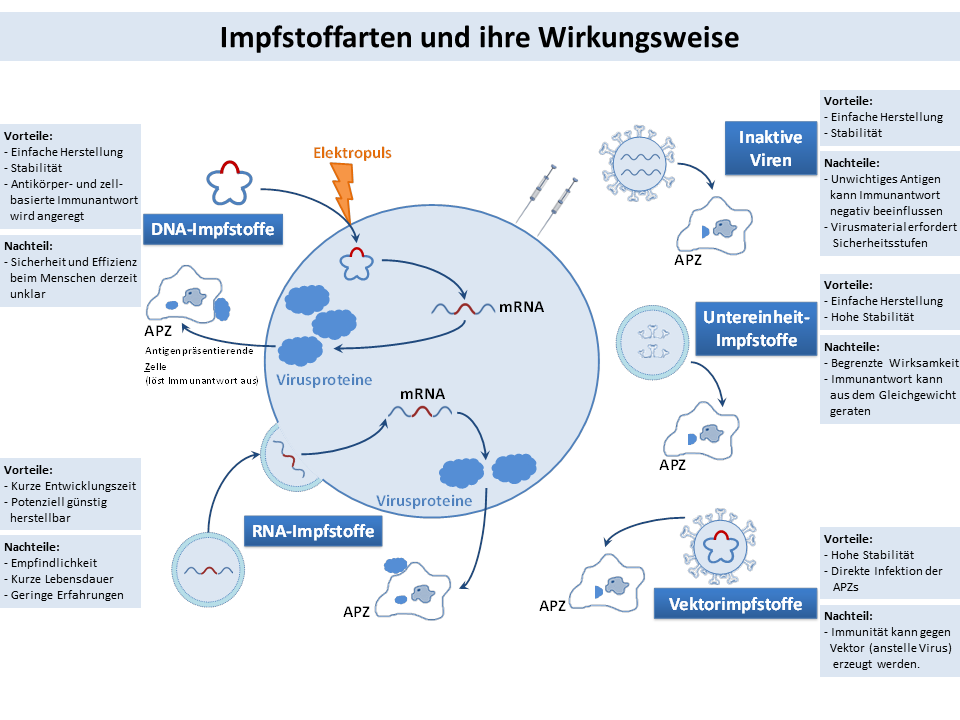
Ein guter Überblick über die Schritte bis zur Zulassung eines Impfstoffs sowie die aktuell in der Erprobung befindlichen Impfstofftypen findet sich auf der Internetseite des Verbands forschender Arzneitmittelhersteller (vfa) [21c,d].
Fragen und Antworten zu den verschiedenen Impfstoffen
Sind die neuartigen RNA- und Vektorimpfstoffe ausreichend abgesichert?
Die zugelassenen mRNA-Impfstoffe wurden mittlerweise an mehr als eine Milliarde Menschen verimpft, die Vektorimpfstoffe von AstraZeneca und Johnson&Johnson an fast 2 Milliarden Menschen. Die sehr gute Verträglichkeit und hohe Wirksamkeit kann durch diese breite, weltweite Anwendung als nachgewiesen angesehen werden.
Sind klassische Totimpfstoffe verträglicher und wirksamer als die neuartigen RNA- und Vektorimpfstoffe?
Die Verträglichkeit der neuen RNA- und vektorbasierten Impfstoffe ist sehr hoch. Mögliche Langzeitfolgen sind in hohem Maße unwahrscheinlich, dass die Wirkstoffe nach kurzer Zeit rückstandsfrei abgebaut werden. Somit sind ungewollte, langfristige Wirkungen auf Körperzellen ausgeschlossen. Impfstoffe, die nach klassischen Totimpfstoffverfahren gewonnen werden, bergen hier möglicherweise höhere Risiken von Autoimmunreaktionen. Aufgrund Ihrer breiteren Immunantwort (das Immunsystem muss auf das ganze Virus reagieren) und des notwendigen Einsatzes von Wirkstoffverstärkern ist das Auftreten von Überreaktionen und Nebenwirkungen im Fall des unberechenbaren Coronavirus deutlich schwieriger zu kontrollieren. Wie sicher die in der Zulassung befindlichen Totimpfstoffe sind, die nach den „klassischen“ Verfahren gewonnen werden, ist derzeit noch in Untersuchung. Bezüglich Wirksamkeit zeichnet sich auf Basis derzeit vorliegenden Studiendaten insgesamt eine deutlich schlechtere Schutzwirkung als bei den zugelassenen mRNA-Impfstoffen ab. Inwieweit die breitere Immunantwort der klassisch gewonnenen Corona-Totimpfstoffe einen Vorteil beim Schutz ggü. der Omikron-Mutation bietet, kann aktuell noch nicht beurteilt werden.
Macht es Sinn, auf die Freigabe und Verfügbarkeit klassischer Totimpfstoffe zu warten?
Ein klares Nein! Wie oben ausgeführt, sind die derzeitigen RNA-Impfstoffe in hohem Maße wirksam und sicher. Deren Modifizierung bei Wirksamkeitsverlust ggü. neuen Mutationen wird zudem deutlich schneller gelingen als bei klassischen Impfstoffen. Auch die aktuell verfügbaren Vektor- und mRNA-Impfstoffe schützen vor einem schweren Krankheitsverlauf bei Infektion mit der Virusvariante Omikron. Allerdings ist hier bei Erwachsenen spätestens 5-6 Monate nach vollständig abgeschlossenem Impfschema eine Auffrischung („Booster“-Impfung) mit einem mRNA-Impfstoff erforderlich, um eine Schutzwirkung von 75% aufrechtzuerhalten.
Verändern RNA-Impfstoffe mein Erbgut?
Nein, das ist definitiv nicht möglich. Aufgrund ihrer „Reaktivität“ kann die eingeschleuste mRNA nicht in die Nähe der Zellkern-DNA kommen. Zudem muss für eine Erbgutveränderung mRNA in DNA umgeschrieben werden und diese in die humane DNA eingebaut werden. Die hierfür notwendigen Enzyme (die sogen. reverse Transkriptase und die Integrase) sind in der Zelle nicht vorhanden. Retroviren wie HIV bringen diese mit, um ihr Erbgut einzubauen, die mRNA- und Vektor-Impfstoffe natürlich nicht.
Medikamente [20a]
Bisher gibt es keine ausreichend wirksame medikamentöse Therapie für COVID-19. Zur kurzfristigen Bereitstellung von Behandlungsmöglichkeiten werden bereits für andere Erkrankungen zugelassene Medikamente hinsichtlich Wirksamkeit gegen das neue Corona-Virus geprüft. Auch hier werden 3 Ansätze verfolgt:
- Antivirale Medikamente: Gegen Ebola, HIV oder andere Virusinfektionen entwickelte Wirkstoffe könnten auch gegen SARS-CoV-19 wirken. Sie hemmen die Vermehrung der Viren. Dabei rückten zunächst bekannte Anti-Malaria-Medikamente, Chloroquin und Hydroxychloroquin aufgrund ihrer antiviralen Wirkung in den Fokus [20b]. Entgegen erster vielversprechender Laborergebnisse zeigten anschließende breit angelegte klinische Studien keine Wirksamkeit ggü. COVID-19, sondern eher schädigende Wirkung [20c]. Erfolgversprechender zeigten sich anfänglich die Studien mit dem Anti-Ebola-Medikament Remdesivir [20d]. Hier wurden Verkürzungen in der Behandlungszeit von Schwererkrankten von 4 Tagen berichtet [20e]. Spätere Untersuchungen zeigten allerdings, dass Remdesivir die Produktion der Virus-RNA nur teilweise blockiert und das für die RNA-Verdopplung verantwortliche Enzym nach einer Fehlerkorrektur weiterarbeitet [20f].
- Immunmodulatoren: Sie schützen das Immunsystem vor Überreaktionen. Diese Wirkstoffe zielen darauf ab, den Krankheitsverlauf abzumildern, indem sie die körpereigene Abwehrreaktion regulieren und ggf. dämpfen. Derartige Wirkstoffe werden heute bei rheumatischen Erkrankungen oder entzündlichen Darmerkrankungen eingesetzt. Gesteigertes Interesse ziehen Immunglobuline auf sich, die aus menschlichem Blutplasma gewonnen werden [21a]. Aufgrund ihrer Fähigkeit, Überreaktionen des Immunsystems zu reduzieren und dieses gleichzeitig bei der Wiedererkennung und Zerstörung von Krankheitserregern zu unterstützen, sehen Forscher hier aktuell große Therapiepotenziale. Zur Gewinnung von Präparaten aus dem Blutplasma geheilter COVID-19 Patienten hat sich eine industrieübergreifende Initiative gebildet [21b].
- Medikamente für Lungenkranke: Da COVID-19 in hohem Maße die Lunge in Mitleidenschaft zieht, könnten Medikamente, die der Vernarbung von Lungengewebe entgegenwirken, einen günstigeren Krankheitsverlauf unterstützen. Im Fokus sind dabei Arzneimittel, die gegen die sogenannte zystische Lungenfibrose, eine angeborene Stoffwechselerkrankung, zugelassen sind.
Parallel zur Wirksamkeitsprüfung bereits zugelassener Medikamente arbeiten Wissenschaftler mit Hochdruck an maßgeschneiderten, neuen Wirkstoffen. Ein interessanter und wichtiger Meilenstein war die Entschlüsselung des Hauptproteins des aktuellen Corona-Virus, welche Forschern am Helmholtz-Zentrum Berlin kürzlich gelang [22]. Ein hochattraktiver Ansatz der aktuellen Wirkstoffforschung fokussiert auf die Hemmung der Virusvermehrung [23].
Eine Reihe hochwirksamer antiviraler Wirkstoffe weisen Polyacetylenstrukturen auf [24]. Diese Strukturen sind heute mit Hilfe moderner chemischer Reaktionsmethoden synthetisch einfach zugänglich [25]. Der Weg von ersten Modellsubstanzen und Wirkstoffen im Labormaßstab bis hin zu einem neuen, zugelassenen Medikament wird voraussichtlich mehrere Jahre in Anspruch nehmen.
Aktuelle Informationen und Nachrichten rund um Forschungsaktivitäten zu Corona können Sie dem Informationsportal des HZI in Braunschweig entnehmen: https://www.helmholtz.de/aktuell/coronavirus-sars-cov-2/
Quellen
[20a] Helmholtz-Institut für Infektionsforschung Braunschweig, Sars-CoV-2, Wann wird es einen Impfstoff gegen das neuartige Coronavirus geben?, Web-Publikation, 2020, https://www.helmholtz.de/gesundheit/wann-wird-es-einen-impfstoff-gegen-das-neuartige-coronavirus-geben/
[20b] M. R. Mehra, S. S. Desai, F. Ruschitzka, A. N. Patel, The Lancet 2020, 1-10. Published: May 22, 2020, DOI:https://doi.org/10.1016/S0140-6736(20)31180-6
[20c] BR 24, Web-Publikation vom 18.06.2020, Malaria-Mittel Hydroxychloroquin bei Covid-19 unwirksam.
https://www.br.de/nachrichten/wissen/corona-malaria-mittel-hydroxychloroquin-bei-covid-19-unwirksam,RtghbZ4
[20d] BR24, Web-Publikation vom 03.07.2020, Studie: Remdesivir verkürzt Behandlung von Covid-19-Patienten.
https://www.br.de/nachrichten/wissen/studie-remdesivir-verkuerzt-behandlung-von-covid-19-patienten,RxeJSBe
[20e] J.H. Beigel, K.M. Tomashek, L.E. Dodd, A.K. Mehta, B.S. Zingman, A.C. Kalil, E. Hohmann, H.Y. Chu, A. Luetkemeyer, S. Kline, D. Lopez de Castilla, R.W. Finberg, K. Dierberg, V. Tapson, L. Hsieh, T.F. Patterson, R. Paredes, D.A. Sweeney, W.R. Short, G. Touloumi, D.C. Lye, N. Ohmagari, M. Oh, G.M. Ruiz-Palacios, T. Benfield, G. Fätkenheuer, M.G. Kortepeter, R.L. Atmar, C.B. Creech, J. Lundgren, A.G. Babiker, S. Pett, J.D. Neaton, T.H. Burgess, T. Bonnett, M. Green, M. Makowski, A. Osinusi, S. Nayak, and H.C. Lane, N. Engl. J. Med. 2020, 1-12, DOI: 10.1056/NEJMoa2007764.
https://www.nejm.org/doi/pdf/10.1056/NEJMoa2007764?articleTools=true
[20f] G. Kokic, H. S. Hillen, D. Tegunov, C. Dienemann, F. Seitz, J. Schmitzova, L. Farnung, A. Siewert, C. Höbartner, P. Cramer, Nature Communications 2021, 12, 279. https://doi.org/10.1038/s41467-020-20542-0
[21a] Pressemitteilung Biotest AG, 03.04.2020, Biotest AG: Biotest entwickelt mit Trimodulin einen neuen Therapieansatz für Covid-19 Patienten mit schwerem Verlauf, Dreieich, 2020,
https://www.biotest.com/de/de/investor_relations/news_und_publikationen_/biotest_pressemitteilungen/press_detail.cfm?instance_ID=2769&cmfaction=xmldetail.xmldetail.detailview&showdetails=1938939
[21b] Pressemitteilung Biotest AG, 06.04.2020, Biotest stellt lebensrettende Medikamente aus Plasma von geheilten COVID-19 Patienten her und beteiligt sich dazu an Industrie-übergreifender Initiative, Dreieich, 2020,
https://www.biotest.com/de/de/investor_relations/news_und_publikationen_/biotest_pressemitteilungen/press_detail.cfm?instance_ID=2769&cmfaction=xmldetail.xmldetail.detailview&showdetails=1939973
[21c] vfa. Die forschenden Pharmaunternehmen, Impfstoffe zum Schutz vor Covid-19, der neuen Coronavirus-Infektion, Web-Publikation, 18.08.2020, https://www.vfa.de/de/arzneimittel-forschung/woran-wir-forschen/impfstoffe-zum-schutz-vor-coronavirus-2019-ncov
[21d] vfa. Die forschenden Pharmaunternehmen, Impfstoffe zum Schutz vor der Coronavirus-Infektion Covid-19, Web-Publikation, 30.12.2020,
Impfstoffe gegen Coronavirus – aktueller Entwicklungsstand | vfa
[21e] T. Dingermann, Pharmazeutische Zeitung 2020, Web-Publikation 21.12.2020,
Produkteigenschaften: Mehr Details zum Biontech-Impfstoff | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de)
[21f] T. Dingermann, Pharmazeutische Zeitung 2020, Web-Publikation 08.12.2020,
Produkteigenschaften: Mehr Details zum Moderna-Impfstoff | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de)
[21g] S. Siebenand, Pharmazeutische Zeitung 2020, Web-Publikation 24.08.2020,
Nase vorn: Nasale Coronavirus-Impfung schlägt Injektion | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de)
[21h] C. Homann-Jeddi, Pharmazeutische Zeitung 2020, Web-Publikation 30.12.2020, Covid-19: Astra-Zeneca-Impfstoff in Großbritannien zugelassen | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de)
[21i] C. Homann-Jeddi, Pharmazeutische Zeitung 2020, Web-Publikation 11.12.2020, Vektorimpfstoff-Kombination: Astra-Zeneca plant Studie mit russischen Impf | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de)
[21j] vfa. Die forschenden Pharmaunternehmen, Impfstoffe zum Schutz vor der Coronavirus-Infektion Covid-19, Web-Publikation, 06.01.2021,
Impfstoffe gegen Coronavirus – aktueller EntwicklungsstandImpfstoffe gegen Coronavirus – aktueller Entwicklungsstand | vfa | vfa
[21k] Y. Dong, T. Dai, Y. Wei et al., Sig. Transduct. Taget. Ther. 2020,5, 237.
[21l] M. Groß, Nachr. Chem. 2021, 69 (2), 50-53.
[21m] Pharmazeutische Zeitung 2021, Web-Publikation 21.01.2021, Covid-19-Vektorimpfstoff: Russland will EU-Zulassung für Sputnik-V | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de)
[21n] Ärzteblatt 2021, Web-Publikation 02.02.2021, Sputnik V: Russischer Impfstoff erzielt auch im Alter hohe… (aerzteblatt.de)
[21o] D. Y. Logunov, I. V. Dolzhikova, D. V. Shcheblyakov, A. I. Tukhvatulin, O. V. Zubkova, A. S. Dzharullaeva et. al., Lancet 2021, 1-11, DOI: 10.1016/S0140-6736(21)00234-8, published online February 2, 2021
[21p] Ärzteblatt 2021, Web-Publikation 01.03.2021, FDA-Zulassung: Was den Johnson & Johnson-Impfstoff von den anderen… (aerzteblatt.de)
[21q] D. Hüttemann, Pharmazeutische Zeitung 2021, Web-Publikation 16.02.2021, Nur eine Dosis nötig: Janssen beantragt EU-Zulassung für Covid-Impfstoff | PZ – Pharmazeutische Zeitung (pharmazeutische-zeitung.de
[21r] L. Bachelot-Fontaine, J. Drumm, Report der Firma Valneva 18.10.2021, 1-4, 2021_10_18_VLA2001_Phase3_Results_PR_EN_Final.pdf (valneva.com)
[21s] Unternehmenspublikation der Fa. Novavax, Web-Publikation 17.12.2021, Coronavirus-Impfstoff-Updates | COVID-19-Impfstoff Neueste Nachrichten | Novavax
[22] Helmholtz-Zentrum Berlin, SARS-CoV-2, Blaupause für einen Wirkstoff gegen das neue Coronavirus, Web-Publikation, 2020, https://www.helmholtz.de/gesundheit/blaupause-fuer-einen-wirkstoff-gegen-das-neue-coronavirus/
[23] Linlin Zhang, Daizong Lin, Xinyuanyuan Sun, Ute Curth, Christian Drosten, Lucie Sauerhering, Stephan Becker, Katharina Rox, Rolf Hilgenfeld. Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved alpha-ketoamide inhibitors. Science 2020, DOI: 10.1126/science.abb3405.05.
[24] P. Siemsen, R.C. Livingston, F. Diederich, Angew. Chem. 2000, 112, 2740-2767; Angew. Chem., Int. Ed. 2000, 39, 2632-2657.
[25] P. Siemsen and B. Felber in Handbook of C-H Transformations, Vol. 1, G. Dyker (Ed.), Wiley-VCH: Weinheim 2005, 53-62. Inkl. darin zitierte Publikationen.
